Usted está aquí
Artículo
Actuación de enfermería ante la Hipertermia Maligna.
Enferm. anest.-reanim. ter. dolor (Internet) Vol.3 nº2 2018 / ISSN: 2529-9670
Autor: : Mont Esbert, M.*; Castillo Lucas, R.*
* Unidad de quirófano. Hospital General Mateu Orfila. Maó. España).
Contacto: montsesbert@gmail.com
RESUMEN
Objetivos: Adquirir los conocimientos necesarios para actuar con la máxima rapidez ante una posible crisis de Hipertermia Maligna. Método: Búsqueda bibliográfica en bases de datos PUBMED y CUIDEN desde 1995 hasta la actualidad. Conclusiones: La agilización de las actuaciones ante la Hipertermia Maligna y su conocimiento disminuyen la mortalidad del paciente y mejoran la calidad de los cuidados. Palabras clave (MeSH/DeSC): Hipertermia maligna, dantroleno, relajantes musculares, anestesia general.
ABSTRACT
Objective: To acquire the necessary knowledge in order to act with the utmost promptness in a possible Malignant Hyperthermia crisis. Method: Bibliographical research in PUBMED and CUIDEN databases from 1995 until now. Conclusions: Speeding up the actions when facing Malignant Hyperthermia, and its knowledge, reduces patients mortality and improves care quality. Key Words: Malignant Hyperthermia, dantrolene, muscle relaxants, general anesthesia
INTRODUCCION
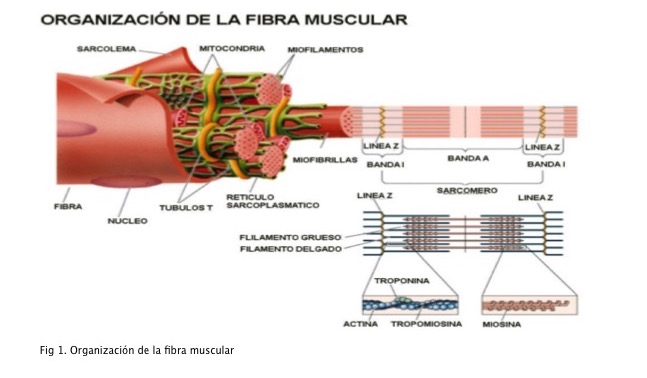
La Hipertermia Maligna (HM) o hiperpirexia maligna es un síndrome de carácter hereditario que afecta fundamentalmente al músculo esquelético y que ocasiona una rápida elevación de la temperatura corporal y contracciones musculares agudas cuando la persona afectada es sometida a anestésicos inhalatorios y/o relajantes musculares (succinilcolina). La HM está causada por una incapacidad de la fibra muscular para controlar las concentraciones de calcio (Ca2+) en su interior, y que implica la existencia de una alteración generalizada de la permeabilidad de la membrana, tanto a nivel celular como subcelular.1 (Figura 1)
Su mortalidad es elevada si no se actúa correctamente. Actualmente existe un tratamiento específico para la hipertermia maligna que es el dantroleno.
Esta rara enfermedad es hereditaria, autosómica dominante, por lo que sólo se requiere un padre portador. También puede estar asociada a enfermedades musculares. Habitualmente es debido a la mutación del gen codificador del receptor rianodínico, en el cromosoma 19.
También existe una asociación a mutaciones del gen que codifica los canales del Ca2+.
Esta enfermedad se desencadena por la administración de anestésicos inhalatorios volátiles halogenados (halotano, enflurano, sevoflurano, isoflurano, desflurano y methoxiflurano) así como también la succinilcolina (relajante muscular). 2
La incidencia exacta no se conoce, sin embargo se acepta la cifra de 1/14.000 anestesias en niños y 1/40.000 en adultos, como promedio más fiable. Dicha incidencia puede variar según la distribución geográfica y el porcentaje de familias susceptibles a HM en la zona estudio. En España es poco frecuente en la población autóctona pero hay que tener en cuenta que el aumento de la inmigración puede elevar la posibilidad de encontrar pacientes susceptibles.
La HM es más frecuente en niños o en adultos jóvenes no obstante se han dado casos excepcionales desde los 2 meses a los 70 años.
La prevalencia es mayor en hombres (68%) que en mujeres (32%).3
La HM está causada por una incapacidad de la fibra muscular para controlar las concentraciones de Ca2+ en su interior, debido a una alteración generalizada de la permeabilidad de la membrana2. La elevación de la concentración de Ca2+ libre es el desencadenante de la destrucción de la célula muscular, lo que ocasionará una contracción permanente, liberación de calor y un hipermetabolismo que conduce a un aumento del consumo de oxígeno (O2) y de producción de dióxido de carbono (CO2).
El principal problema que presenta la HM es su identificación ya que los signos y síntomas que se presentan no son específicos.4
Las crisis generalmente se presentan de forma aguda tras la inducción anestésica, pero en ocasiones pueden aparecer varias horas después de haberse iniciado la anestesia.
Durante la crisis de HM tiene lugar un fuerte incremento del consumo de oxígeno y la producción de lactato, apareciendo un aumento de la acidosis respiratoria y metabólica, rigidez muscular, estimulación del sistema nervioso simpático e incremento de la permeabilidad celular. Se produce un descenso del pH, presión parcial de oxígeno (PO2) y un aumento de presión parcial de dióxido de carbono (PCO2), potasio (K+) y temperatura. El incremento del metabolismo es un intento por parte de la fibra muscular de producir suficiente ATP.3,4
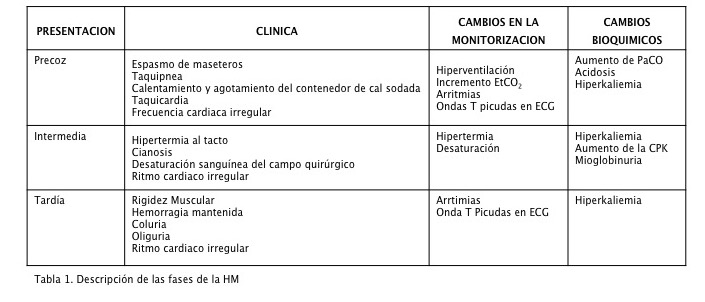
A continuación se detalla la clínica más relevante.5 (Tabla 2)
Hipercapnia. El signo más precoz que aparece es un aumento del CO2 espirado en la capnografía (si el paciente ventila espontáneamente, se observa una hiperventilación).
Hiperventilación y sudoración. Si el paciente está ventilando espontáneamente, se observa una taquipnea intensa con profusa sudoración, junto con el rápido y excesivo calentamiento de la cal sodada, que se decolora en el canister. Finalmente, se produce una hipoventilación, incluso puede aparecer apnea.
Taquicardia. Más del 90% de todos los casos de HM presentan este signo durante los primeros 30 minutos de anestesia. Casi siempre aparece antes que la fiebre e incluso de la rigidez. Cuando no se detecta un aumento de la concentración de CO2 espirado (ETCO2), una taquicardia súbita e inexplicable suele ser el primer signo del síndrome de HM. En ese momento, una gasometría arterial pondrá en evidencia la gran alteración existente.
Alteraciones en el electrocardiograma (ECG). Junto con la taquicardia, o poco después de su aparición, con frecuencia se producen arritmias ventriculares multifocales pudiendo desencadenar una parada cardíaca.
Inestabilidad hemodinámica. La presión arterial sistólica varía más de lo esperado de una toma a otra, aumentando lentamente primero, debido a un aumento del gasto cardíaco, y descendiendo bruscamente después, desencadenando un severa hipotensión tras la cual sobreviene la parada cardíaca.
Rigidez. Aunque su aparición no es constante, este signo suele presentarse en los primeros momentos de la crisis de HM, casi siempre tras la administración de succinilcolina. La rigidez suele verse precedida de una fasciculación masiva y puede evolucionar hacia una situación similar al rigor mortis.
La rigidez se manifiesta primero en los músculos maseteros, haciendo muy difícil, o imposible, la intubación. En algunos pacientes la rigidez tarda en aparecer, incluso puede presentarse después de finalizar el acto anestésico. El espasmo del músculo masetero, por sí mismo, no está relacionado siempre con la hipertermia maligna, pero la mayoría de los clínicos aconsejan terminar el acto anestésico-quirúrgico de inmediato y estudiar detenidamente al paciente.
Moteado cianótico. Con frecuencia se observa un enrojecimiento de la piel en la parte anterior del cuello y tórax. Casi siempre éste va seguido de un peculiar moteado cianótico, debido a un espasmo arteriolar temprano.
Fiebre. La fiebre en el síndrome de HM es debida a una disminución de la pérdida de calor secundaria al vasoespasmo periférico y a una producción excesiva de calor en los músculos. El aumento del ETCO2, la taquicardia y la rigidez muscular, preceden a la hipertermia, por lo tanto es un signo relativamente tardío. La temperatura se eleva por encima de los 40Cº, aumentando la mortalidad.
Alteraciones de laboratorio. Poco después de la administración del agente desencadenante, los pacientes afectados muestran elevaciones de la glucosa, lactato y piruvato en plasma.
Se produce una caída del pH y un aumento del déficit de bases. Junto con estas alteraciones, se manifiestan aumentos de los niveles séricos de K+, sodio (Na+) y cloro (Cl-). Existen otras alteraciones que no se detallan.
Entre las complicaciones tardías se encuentran la insuficiencia renal aguda, la coagulopatía de consumo (CID), el edema pulmonar agudo, el edema cerebral agudo y el edema muscular agudo.
Algunas crisis de HM comienzan en la Unidad de Recuperación Postanestésica o incluso en la planta de hospitalización, desencadenadas por los escalofríos, el dolor o la agitación. No suelen ser tan graves como las intraoperatorias, pero se han descrito casos de muerte. Los paciente afectados presentan fiebre moderada, taquicardia, discreta cianosis, hiperventilación y agitación.
OBJETIVO
Una HM se considera una urgencia vital donde el tiempo transcurrido va en contra del pronóstico del paciente.
Los objetivos son identificar los signos y síntomas de la HM y adquirir los conocimientos necesarios para actuar con la máxima rapidez ante una posible crisis.
PROCEDIMIENTO
Ante la sospecha de una HM será el anestesista quien indicará los pasos a seguir:
· Solicitar ayuda, finalizar la cirugía y eliminar los agentes desencadenantes.
· Cambiar las tubuladuras del respirador y la cal sodada y ventilar con O2 al 100% con un volumen mínimo tres veces superior al empleado hasta ese momento con el fin de intentar eliminar el exceso de anhídrico carbónico producido por el hipermetabolismo muscular5.
· Administrar dantroleno sódico 2,5mg/kg cada 5-10 minutos hasta que ceda el cuadro (dosis total:10mg/kg). Administrar por vía venosa central para evitar la irritación venosa periférica debido al pH elevado lo que dificulta la disolución de dicho fármaco. El dantroleno se dispensa en dos viales (uno con la medicación liofilizada y otro con el agua para su inyección). Una vez preparado proteger de la luz y administrar antes de 6 horas. Para un adulto de 70kg son necesarios 7 viales como medida de choque. Se considera que la cantidad de 36 ampollas es el stock mínimo que cada hospital debe tener disponible de forma inmediata.3,6
· Obtener gasometrías y analíticas seriadas para corregir el pH (corregir solamente en un 50%) y la hiperpotasemia, realizar sondaje vesical y monitorizar la temperatura central.5,7
· Controlar la fiebre mediante suero salino 0,9% frío a 15ml/kg cada 15 minutos, lavado de estómago, vejiga, recto y cavidades abiertas con suero salino frío, enfriamiento cutáneo con hielo o manta hipotérmica. El descenso de la temperatura puede ser intensificado administrando al paciente clorpromacina, que contribuye a la vasodilatación periférica. El enfriamiento debe suspenderse a la temperatura de 38-39ºC, evitando el enfriamiento extremo ya que disminuye la capacidad de pérdida de calor.7
· Los trastornos del ritmo deben ser tratados si no ceden con la desaparición de la hipertermia y la acidosis.5,7
· Valorar la posibilidad de monitorización hemodinámica invasiva (presión arterial y presión venosa central)
· Trasladar al paciente a UCI una vez estabilizado y continuar el tratamiento con dantroleno a 2,5mg/kg cada 4h hasta la desaparición del cuadro. Posteriormente continuar con 4mg/kg/día durante 48 horas para prevenir las posibles recurrencias. 6,7
CONCLUSIONES
Debido a la urgencia del tratamiento y la gravedad de la enfermedad es importante el trabajo en equipo. Para garantizar la seguridad del paciente se recomienda que el Dantroleno se encuentre en el bloque quirúrgico, siendo de fácil localización y acceso conocido por el personal, además de tener el stock suficiente para administrar un tratamiento completo.
Actuar con la misma rapidez que si de una parada cardíaca se tratase y seguir un protocolo de actuación que debe ser conocido por todo el personal de quirófano.
La agilización de las actuaciones y su conocimiento disminuyen la mortalidad del paciente mejorando la calidad de los cuidados.
BIBLIOGRAFIA
- Torres, Luis M. Anestesia inhalatoria. En: Gómez-Herreras; JL, Vegas H; Tamayo, E. Tratado de Anestesia y Reanimación. 1ª ed. Madrid: Arán Ediciones, SL; 2001. pág. 1657-1686. Cap. 57.
- Correira, ACC; Silva, PCB; Silva, BA. Hipertermia maligna: aspectos moleculares y clínicos. Revista Brasileira de Anestesiología. 2012; vol 62 (nº 6) p. 828-837.
- Ortiz Gómez, JR. Anestesia en la hipertermia maligna. Revista Española de Anestesiología y Reanimación. 2008; vol 55 (nº3) p.165-174.
- Carrillo-Esper, R; Lázaro-Santiago, G; Nava-López, JA. Hipertermia maligna. Conceptos actuales. Revista Mexicana de Anestesiología. 2013; vol 36 (nº 3) pág. 185-192.
- Torres, Luis M. Complicaciones durante la anestesia. En: Caba, F. ; Campos, JM; Herrero, A; Caballero, V; Neira, F; González-Machado, JL. Tratado de Anestesia y Reanimación. 1 ed. Madrid: Arán Ediciones, SL; 2001. p. 2023-2060.
- Pastó Cardona, L; Casals Caus, P; Barroso de Fuenmayor, E; Llop Talaverón, JM. Dantroleno intravenoso en hipertermia maligna y síndrome neuroléptico maligno: protocolo de utilización. Revista Farm Hosp. 1995; vol 19 (nº 2) p. 95-98.
- Enciso Nano, Jorge. Revisión. Bibliográfica de la Hipertermia Maligna. Rev. Horizonte médico, 2007, vol/ (nº 1), pág 47-55.
- MHAUS. Malignant Hyperthermia Association of the United States [Internet]. Sherburne, New York; 1981, [fecha de consulta 15 de marzo de 2018]. Disponible en: http://www.mhaus.org/.
- MedlinePlus. [base de datos en Internet]. Bethesda: National Library of Medicine; [fecha de consulta 16 de marzo de 2018]. Disponible en: http://www.medlineplus.gov/spanish/.
